行業(yè)新聞
香港進(jìn)口物流:醫(yī)療器械A(chǔ)ED進(jìn)口申報(bào)要求
作者:飛龍世紀(jì)物流 發(fā)布時(shí)間:2024-01-10 字體:大 中 小
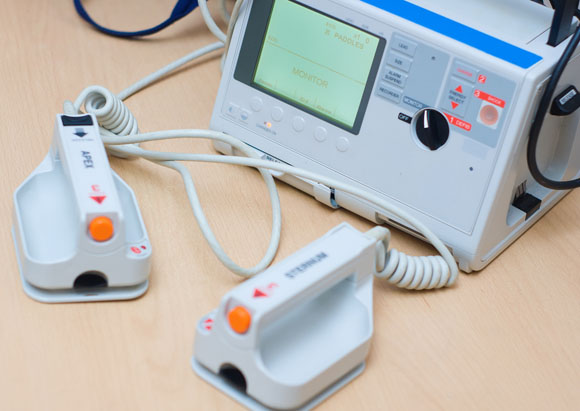
醫(yī)療急救設(shè)備AED(英文為Automated External Defibrillator)是自動(dòng)體外除顫器的英文簡(jiǎn)稱,又稱自動(dòng)體外電擊器、自動(dòng)除顫器、心臟除顫器等。其進(jìn)口申報(bào)要求如下:
一、歸類和稅率
AED的歸類要素為品名、用途和原理,根據(jù)《進(jìn)出口稅則商品及品目注釋》,其90.18品目注釋列明,可利用電流停止心臟纖維性顫動(dòng)的心臟除顫器,屬于本品目其他電氣醫(yī)療設(shè)備。根據(jù)《中華人民共和國(guó)海關(guān)進(jìn)出口稅則》(2022年版),AED主要功能用于心臟除顫,商品編碼建議歸入90189099,進(jìn)口關(guān)稅最惠國(guó)為0%、普通為17%,進(jìn)口增值稅為13%。
二、規(guī)范申報(bào)要求
AED進(jìn)口申報(bào)要素為品名、用途、原理、中文及外文品牌名稱,型號(hào)及醫(yī)療器械注冊(cè)編號(hào)。
按照規(guī)定,進(jìn)口的醫(yī)療器械應(yīng)當(dāng)有中文說(shuō)明書(shū)、中文標(biāo)簽。說(shuō)明書(shū)、標(biāo)簽應(yīng)當(dāng)符合《醫(yī)療器械監(jiān)督管理?xiàng)l例》規(guī)定以及相關(guān)強(qiáng)制性標(biāo)準(zhǔn)的要求,并在說(shuō)明書(shū)中載明醫(yī)療器械的原產(chǎn)地以及境外醫(yī)療器械注冊(cè)人、備案人指定的我國(guó)境內(nèi)企業(yè)法人的名稱、地址、聯(lián)系方式。沒(méi)有中文說(shuō)明書(shū)、中文標(biāo)簽或者說(shuō)明書(shū),標(biāo)簽不符合本條規(guī)定的,不得進(jìn)口。
三、特殊監(jiān)管規(guī)定
(一)注冊(cè)管理
根據(jù)《醫(yī)療器械分類目錄匯編2022版》,AED屬于第三類醫(yī)療器械,國(guó)家對(duì)第三類醫(yī)療器械實(shí)行產(chǎn)品注冊(cè)管理,進(jìn)口的AED應(yīng)當(dāng)按規(guī)定已完成注冊(cè)。申請(qǐng)注冊(cè)應(yīng)當(dāng)提交下列資料:
1.產(chǎn)品風(fēng)險(xiǎn)分析資料;
2.產(chǎn)品技術(shù)要求;
3.產(chǎn)品檢驗(yàn)報(bào)告;
4.臨床評(píng)價(jià)資料;
5.產(chǎn)品說(shuō)明書(shū)以及標(biāo)簽樣稿;
6.與產(chǎn)品研制、生產(chǎn)有關(guān)的質(zhì)量管理體系文件;
7.證明產(chǎn)品安全、有效所需的其他資料。
申請(qǐng)第三類醫(yī)療器械產(chǎn)品注冊(cè)應(yīng)當(dāng)向國(guó)務(wù)院藥品監(jiān)督管理部門提交注冊(cè)申請(qǐng)資料。醫(yī)療器械注冊(cè)申請(qǐng)人應(yīng)當(dāng)確保提交的資料合法、真實(shí)、準(zhǔn)確、完整和可追溯。
向我國(guó)境內(nèi)出口第二類、第三類醫(yī)療器械的境外注冊(cè)人,由其指定的我國(guó)境內(nèi)企業(yè)法人向國(guó)務(wù)院藥品監(jiān)督管理部門提交注冊(cè)申請(qǐng)資料和注冊(cè)申請(qǐng)人所在國(guó)(地區(qū))主管部門準(zhǔn)許該醫(yī)療器械上市銷售的證明文件。其產(chǎn)品須經(jīng)注冊(cè)檢測(cè)合格并取得“醫(yī)療器械注冊(cè)證”,方可進(jìn)口。
(二)注冊(cè)人義務(wù)
按照規(guī)定,醫(yī)療器械注冊(cè)人應(yīng)當(dāng)履行下列義務(wù):
1.建立與產(chǎn)品相適應(yīng)的質(zhì)量管理體系并保持有效運(yùn)行;
2.制定上市后研究和風(fēng)險(xiǎn)管控計(jì)劃并保證有效實(shí)施;
3.依法開(kāi)展不良事件監(jiān)測(cè)和再評(píng)價(jià);
4.建立并執(zhí)行產(chǎn)品追溯和召回制度;
5.國(guó)務(wù)院藥品監(jiān)督管理部門規(guī)定的其他義務(wù)。
境外醫(yī)療器械注冊(cè)人指定的我國(guó)境內(nèi)企業(yè)法人應(yīng)當(dāng)協(xié)助注冊(cè)人履行前款規(guī)定的義務(wù)。
(三)檢驗(yàn)要求
根據(jù)《醫(yī)療器械監(jiān)督管理?xiàng)l例》規(guī)定,海關(guān)依法對(duì)進(jìn)口醫(yī)療器械實(shí)施檢驗(yàn),聯(lián)網(wǎng)核查其“醫(yī)療器械注冊(cè)證”的真實(shí)性、有效性,驗(yàn)核貨物與證書(shū)內(nèi)容的一致性,檢驗(yàn)不合格的,不得進(jìn)口。國(guó)務(wù)院藥品監(jiān)督管理部門應(yīng)當(dāng)及時(shí)向海關(guān)通報(bào)進(jìn)口醫(yī)療器械的注冊(cè)和備案情況。進(jìn)口口岸所在地海關(guān)應(yīng)當(dāng)及時(shí)向所在地設(shè)區(qū)的市級(jí)人民政府負(fù)責(zé)藥品監(jiān)督管理的部門通報(bào)進(jìn)口醫(yī)療器械的通關(guān)情況。
AED商品編碼對(duì)應(yīng)的監(jiān)管證件代碼為6A,禁止進(jìn)口過(guò)期、失效、淘汰等已使用過(guò)的醫(yī)療器械。
四、溫馨提示
(一)醫(yī)療器械注冊(cè)有效期為5年。有效期屆滿需要延續(xù)注冊(cè)的,應(yīng)當(dāng)在有效期屆滿6個(gè)月前向原注冊(cè)部門提出延續(xù)注冊(cè)的申請(qǐng)。
(二)已注冊(cè)的第二類、第三類醫(yī)療器械產(chǎn)品,其設(shè)計(jì)、原材料、生產(chǎn)工藝、適用范圍、使用方法等發(fā)生實(shí)質(zhì)性變化,有可能影響該醫(yī)療器械安全、有效的,注冊(cè)人應(yīng)當(dāng)向原注冊(cè)部門申請(qǐng)辦理變更注冊(cè)手續(xù)。
(三)出口醫(yī)療器械的企業(yè)應(yīng)當(dāng)保證出口的醫(yī)療器械符合進(jìn)口國(guó)(地區(qū))的要求。
(四)為快速找到附近的AED,可以直接打開(kāi)手機(jī)地圖輸入“AED”,這樣能搜到周圍AED的位置,AED一般被放置在紅色或綠色的盒子里。
相關(guān)新聞
- 出口退運(yùn)物流:退運(yùn)維修貨物如何進(jìn)入保稅區(qū)? 2026-04-27
- 香港海關(guān):5月1日起停用道路貨物資料系統(tǒng) 2026-04-24
- 亞馬遜在深圳啟用全球首個(gè)智能樞紐倉(cāng) 2026-04-23
- 空港中心助力東莞到香港貨運(yùn)時(shí)效提速 2026-04-21
- 油價(jià)致運(yùn)價(jià)彪升 物流企業(yè)營(yíng)運(yùn)成本增加 2026-04-20